Tabla periódica de los elementos
La tabla periódica es un esquema donde se ordenan y clasifican los elementos químicos existentes en el planeta, éstos se encuentran distribuidos en la tabla de acuerdo a las propiedades que poseen.
Lectura .
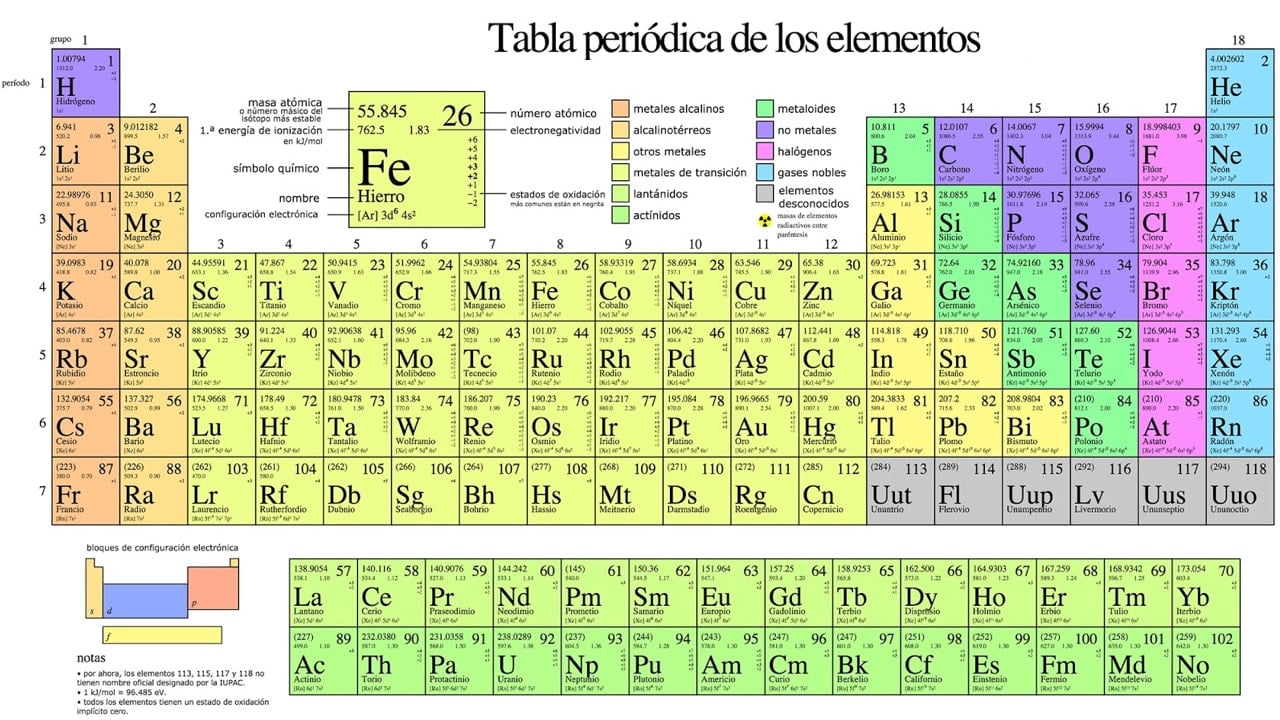
La tabla periódica es un esquema donde se ordenan y clasifican los elementos químicos existentes en el planeta y se encuentran distribuidos de acuerdo a las propiedades que poseen.
Los elementos están ordenados en siete filas llamadas periodos y en 18 columnas verticales llamadas grupos o familias. Están colocados de izquierda a derecha y de arriba a abajo en orden creciente según sus respectivos números atómicos.
Se considera como creador de la tabla periódica al químico ruso Dmitri Ivánovich Mendeléyev, sin embargo, el químico alemán, Julius Lothar von Meyer, también contribuyó a su actual diseño, presentando una tabla ordenada de acuerdo a las propiedades de los átomos. Más adelante, el químico suizo Alfred Werner elaboró el modelo actual realizando algunos cambios a la tabla de Mendeléyev.
Grupos atómicos:
- Grupo 1 (I A): metales alcalinos
- Grupo 2 (II A): metales alcalinotérreos
- Grupo 3 (III B): familia del escandio (tierras raras y actinidos)
- Grupo 4 (IV B): familia del titanio
- Grupo 5 (V B): familia del vanadio
- Grupo 6 (VI B): familia del cromo
- Grupo 7 (VII B): familia del manganeso
- Grupo 8 (VIII B): familia del hierro
- Grupo 9 (VIII B): familia del cobalto
- Grupo 10 (VIII B): familia del níquel
- Grupo 11 (I B): familia del cobre
- Grupo 12 (II B): familia del zinc
- Grupo 13 (III A): térreos
- Grupo 14 (IV A): carbonoideos
- Grupo 15 (V A): nitrogenoideos
- Grupo 16 (VI A): calcógenos o anfígenos
- Grupo 17 (VII A): halógenos
- Grupo 18 (VIII A): gases nobles
Períodos:
Las filas horizontales se llaman períodos. El número de niveles de un átomo determina a que período pertenece. La tabla periódica dispone de 7 períodos, cada elemento se ubica en la tabla conforme a su configuración electrónica.
Bloques:
La tabla periódica se puede dividir en bloques según la secuencia en que se dividen las capas de electrones de los elementos. Los bloques se distribuyen según el orbital en que podría encontrarse el último electrón. Los bloques son: s, p, d, f y g.
Tipos de tabla periódica:
Tabla corta: Es una tabla de ocho columnas que proviene del modelo primario de Mendeleiev-Meyer.
Tabla larga: conocida como tabla de Borh, utiliza la teoría de este químico sobre la distribución electrónica. Esta tabla fue creada por Werner y deriva de la de Meyer. En las verticales están los elementos cuya distribución electrónica coincide. Se extienden los periodos cuarto, quinto y sexto, y se cortan en dos los períodos cortos para ubicar en el medio a las series de los elementos en transición. Generando periodos largos a partir del cuarto período. En esta tabla cada periodo corresponde a la formación de una nueva capa de electrones.
Se han propuesto diferentes tipos de tablas de formas largas:
- Tabla Periódica de 18 columnas.
- Separación en bloques de elementos.
- De forma separada.
Tabla larga extendida:
Representación moderna, ordenado por número atómico creciente, y sigue el llenado de órbitas propuesto por Borh;
- Tabla periódica de 34 columnas,
- Tabla Periódica de 32 columnas, etc.
El primer periodo tiene dos elementos, el segundo y tercero tienen ocho, el cuarto y quinto tienen 18 elementos, el sexto período 32 elementos y el séptimo hasta el momento se agota con 106 elementos.
Le puede interesar:
Grupos de Elementos de la Tabla Periódica
Tabla periódica de los elementos
¿Tiene algún comentario? deje el suyo más abajo...